IVDR - gemeinsam in Angriff genommen.
Vielleicht wissen Sie bereits, dass Ihr derzeitiger Anbieter seine Nischenprodukte aus dem Sortiment nimmt, und suchen nun nach Alternativen?
Das aktuelle Portfolio von Tecan wurde überprüft, um die Konformität und einen reibungslosen Übergang der verfügbaren Produkte für klinische Labore sicherzustellen. Alle IBL International-Produkte mit CE-IVDD-Kennzeichnung wurden gemäß den in der IVDR festgelegten Klassifizierungsregeln eingestuft, sodass der Verkauf während der geltenden Übergangsfrist weiterhin möglich ist. Kontaktieren Sie uns, um die neueste Version unseres Katalogs zu erhalten und sich einen Überblick über das Portfolio zu verschaffen!
Kontaktieren Sie uns für ein individuelles Angebot und Unterstützung! >
Verfügbarkeit von Immunoassays nach dem 26. Mai 2022
Autoimmunity
Catecholamines / Neurotransmitters
Endocrinology
Saliva Diagnostics
- Cortisol Saliva Luminescence Immunoassay (30221150), 96 tests
- Cortisol Saliva Luminescence Immunoassay Bulk (30221151), 960 tests
- Cortisol Saliva ELISA (RE52611)
- 17beta-Estradiol Saliva Luminescence Immunoassay (RE62141), 96 tests
- 17beta-Estradiol Saliva Luminescence Immunoassay (RE62149), 960 tests
- 17beta-Estradiol Saliva ELISA (30121045)
- Estriol High Sensitive Saliva ELISA (30121046)
- Progesterone Saliva ELISA (RE52281)
- Melatonin direct Saliva ELISA (RE54041)
- Testosterone Saliva ELISA (RE52631)
- Testosterone Saliva Luminescence immunoassay (30191568; IVDR Version von RE62119), 96 tests
- Testosterone Saliva Luminescence immunoassay Bulk (30191569; IVDR Version von RE62039.), 960 tests
Das aktuelle Portfolio von Tecan wurde überprüft, um die Konformität und einen reibungslosen Übergang der verfügbaren Produkte für klinische Labore sicherzustellen. Alle IBL International-Produkte mit CE-IVDD-Kennzeichnung wurden gemäß den in der IVDR festgelegten Klassifizierungsregeln eingestuft, sodass der Verkauf während der geltenden Übergangsfrist weiterhin möglich ist. Kontaktieren Sie uns, um die neueste Version unseres Katalogs zu erhalten.
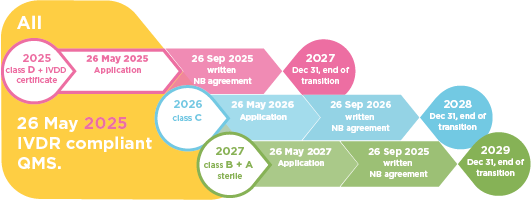
Neue Übergangsfrist für die IVDR.
Die IVDR ist seit Mai 2017 in Kraft und sollte ursprünglich am 26. Mai 2022 wirksam werden.
Die Europäische Kommission hat jedoch die zusätzliche Verordnung (EU) 2024/1860 erlassen, mit der die IVDR geändert wird, um den Übergangszeitraum für die Einführung der IVDR unter bestimmten Bedingungen weiter zu verlängern.
Produkte, die vor dem 26. Mai 2022 mit CE-IVDD gekennzeichnet wurden, dürfen weiterhin für einen verlängerten Zeitraum hergestellt und verkauft werden, allerdings nur, sofern keine wesentlichen Änderungen an der Zweckbestimmung oder dem Design vorgenommen werden. Trotz dieses verlängerten Übergangszeitraums gelten seit dem 26. Mai 2022 bestimmte Anforderungen der IVDR für alle In-vitro-Diagnostika, einschließlich der weiterhin mit CE-IVDD gekennzeichneten Produkte. Zu diesen Anforderungen gehören die Marktüberwachung und die Überwachung nach dem Inverkehrbringen des Produkts, die Vigilanz, die Registrierung der Wirtschaftsakteure sowie die Registrierung der Produkte.
Warum sollten sich klinische Labore dafür interessieren? Hier sind die 5 Hauptgründe die Sie wissen sollten:
- Wissen, wann Sie handeln müssen: Auch wenn es nicht sofort notwendig ist, von "IVDD"- auf "IVDR"-Produkte zu wechseln, sollten die Labore das Ende der Übergangsfristen für die verschiedenen IVDD-Klassen im Auge behalten.
- Rechtzeitig beginnen: Die Laboratorien müssen bedenken, dass sämtliche Produkte, die noch nicht nach der IVDR zertifiziert sind, in naher Zukunft von einer benannten Stelle bewertet werden müssen. Bewertungen durch benannte Stellen sind langwierige und komplexe Prozesse.
- Bleiben Sie informiert: Für Produkte, die noch nicht nach IVDR zertifiziert sind, kann das Labor die Übergangspläne von den Herstellern anfordern.
- Behalten Sie den Überblick über IVDD-Produktänderungen: IVDD-Produkte können auch nach dem 26. Mai 2022 hergestellt und verkauft werden, allerdings sind keine wesentlichen Änderungen des Designs oder des Verwendungszwecks möglich. Sobald das Produkt geändert werden muss, kann es im Anschluss nur mit einem IVDR-Zertifikat verkauft werden. Die Hersteller müssen für geänderte oder neue Produkte eine längere Markteinführungszeit einkalkulieren.
- Keine Panik: Wenn ein Labor von IVDD-Produkten zu IVDR-Produkten wechselt, gibt es im Allgemeinen keine zusätzlichen Anforderungen an den Benutzer. Wenn das Produkt dasselbe ist und nur die Zertifizierung geändert wurde, ist keine neue Validierung erforderlich.
Sind Sie bereit für ein neues Kapitel?
Die Verordnung über In-vitro-Diagnostika (IVDR) ist der neue Rechtsrahmen zur Gewährleistung der Sicherheit und Leistung von In-vitro-Diagnostika auf dem europäischen Markt. Die IVDR ersetzt die derzeitige EU-Richtlinie über In-vitro-Diagnostika (IVDD 98/79/EG) und tritt am 26. Mai 2022 in Kraft. Alle bereits auf dem Markt befindlichen IVDs müssen auf die neue Verordnung umgestellt werden, da es keinen Bestandsschutz für bereits auf dem Markt befindliche Produkte gibt.
Dies bedeutet auch, dass alle derzeit zugelassenen In-vitro-Diagnostika gemäß der IVDR nach den neuen Anforderungen neu zertifiziert werden müssen. Die Hersteller neuer oder bereits auf dem Markt zugelassener IVDs müssen die Einhaltung der neuen IVDR-Anforderungen nachweisen.
Dazu müssen die Hersteller entsprechend der IVDR z. B. klinische Leistungsstudien durchführen und nachweisen, dass die Sicherheit und Leistung des Produkts mit der Risikoklasse oder den Risikovorschriften des Produkts übereinstimmt.
Nach dem neuen IVDR-Klassifizierungssystem werden die Risikoklassen A bis D beschrieben, wobei A für Produkte mit geringem Risiko und D für Produkte mit dem höchsten Risiko für Patienten und die Öffentlichkeit steht.
Das mit der IVDR eingeführte risikobasierte Klassifizierungssystem erfordert die Einbindung einer benannten Stelle bei der Zulassung aller IVDs (außer IVD der Klasse A). Die benannte Stelle arbeitet eng mit dem Hersteller zusammen und ist für die Bewertung aller IVDs verantwortlich.
Es wird erwartet, dass etwa 90 Prozent aller auf dem Markt befindlichen IVDs von einer benannten Stelle bewertet werden müssen. Im Vergleich dazu galt dies bisher für weniger als 15 Prozent der IVDs unter der IVDD.
Ein weiteres Merkmal ist ein neues System zur eindeutigen Produktkennzeichnung von IVDs, die so genannte Unique Device Identification Number (UDI), die sowohl in der Dokumentation, bei der Registrierung als auch auf dem fertigen Produkt zu finden sein wird. Die UDI soll die Rückverfolgbarkeit von Produkten innerhalb der Lieferkette vereinfachen und einen schnellen und effizienten Rückruf von IVDs, die ein Sicherheitsrisiko darstellen, sowie Sichtbarkeit und Transparenz für den Kunden ermöglichen.
Was bedeutet das für die Labore/Kunden?
Das Wichtigste vorweg: Sie als Kunde oder Anwender sind nicht für die Umsetzung des rechtlichen Rahmens und der Anforderungen an die IVD verantwortlich. Jedes Produkt, das Sie nach Mai 2022 mit einer CE-Kennzeichnung auf dem Markt finden, wird den gesetzlichen Vorschriften entsprechen. Das bedeutet jedoch nicht, dass alle Produkte, die bereits auf dem Markt sind, ohne dass die technische Dokumentation fertiggestellt wurde, verschwinden, sondern dass es eine Übergangsfrist gibt, um Produkte nach diesem Termin zu verkaufen und den Versorgungsbedarf zu überbrücken. Der komplexe Regulierungsprozess, die Bedingungen und Regeln sind in Artikel 110 der IVDR zusammengefasst. Einige IVDs mit Richtlinienzertifikat, die von benannten Stellen im Rahmen der Richtlinie ausgestellt wurden, können noch bis zum 27. Mai 2024 auf den Markt gebracht werden.
Nicht alle Hersteller haben eine Vereinbarung mit einer benannten Stelle (ab September 2021), was eine Voraussetzung für CE-IVDR-Produkte (Klasse B, C, D) ist, und nicht alle benannten Stellen sind für die IVDR benannt (fehlender Marktzugang).
Regulierung schlägt Innovation!
Der Markt wird sich verändern und damit auch die Produktpalette. Dies könnte möglicherweise auch Produkte betreffen, die Sie als Kunde für Ihre tägliche Routine in Ihrem Labor kaufen.
Als Anbieter von Routine- und Nischenparametern sind wir bei Tecan daran interessiert, auch weiterhin innovative und Nischenprodukte für besonders seltene Fragestellungen und Krankheiten anzubieten.
Bei der IVDR-Produktzertifizierung stehen wir bei Tecan an vorderster Front. Zusammen mit unserer benannten Stelle haben wir bereits erfolgreich die IVDR-Zertifizierung für ein Produkt erhalten, und viele weitere Produkte sind in Vorbereitung.
Kontaktieren Sie uns für individuelle Angebote und Unterstützung! >