Amyloid-beta (1-42) CSF ELISA
- Regulatorischer Status
- EU: CE
- Kit Größe
- 12 x 8
- Methode
- ELISA
- Inkubationszeit
- 1 x 2h, 1 x 1h, 1 x 30 min.
- Standardbereich
- 7,81 - 125 pg/mL
- Probe / Vorbehandlung
- 5 µL CSF
- Substrat / Isotop
- TMB 450nm
In den letzten 15 Jahren hat die Bestimmung von Amyloid–beta (1–42) sich als ergänzender diagnostischer Marker der Alzheimer–Erkrankung etabliert. Dennoch liegt die klinische Spezifität als auch Sensitiv normalerweise etwas niedriger als 85%. Dies kann man großteils mit der Gauß–Verteilung der Amyloid–beta–Produktion in der Bevölkerung erklären. Dies führt zu falsch positiven Diagnosen in der Gruppe der "wenig" Abeta produzierenden Personen und zu falsch negativen Diagnosen in der Gruppe der "viel" Abeta produzierenden Personen. Normalisiert man jedoch die Amyloid–beta (1–42)-Werte mit der am meisten vorhandenen und stabil produzierten Abeta (1–40)–Isoform, überwindet man dieses Problem und erhöht Signifikant die klinische Trennschärfe auf über 90%. IBL International hatte sich daher zum Ziel gesetzt, qualitative hochwertige Immunoassays für die einfache und akkurate Bestimmung von Amyloid–beta (1–40) and Amyloid–beta (1–42) im Liquor für die optimale Ratio– Bestimmung zu entwickeln, wie es durch exzellente Kreuzreaktivitäten (Tabelle 1) gezeigt wird.
| Peptid | Amyloid–beta (1–40) ELISA | Amyloid–beta (1–42) ELISA |
| Amyloid–beta (1–42) | 0,84% | 100% |
| Amyloid–beta (1–40) | 100% | 0,003% |
| Amyloid–beta (1-38) | 0,01% | 0,57% |
| Amyloid–beta (2-40) | 1,29% | 0,02% |
Tabelle 1
Kreuzreaktivitäten (bestimmt nach Deshpande, SS (1996))
Beide Assays zeigen hervorragende Inter–, Intra–Assay–(Tabelle 2), undInter–Lot–Varianzen (Tabelle 3) hervorgerufen durch rigide, interne Qualitätskontrollen
| Amyloid–beta (1–40) ELISA | Amyloid–beta (1–42) ELISA | |||
| Probe | MW | CV | MW | CV |
| [pg/mL] | [%] | [pg/mL] | [%] | |
| 1 | 4732 | 1,8 | 548 | 3,4 |
| 2 | 9937 | 2,1 | 1023 | 3,0 |
| 3 | 3080 | 4,5 | 849 | 3,0 |
| 4 | 10497 | 1,9 | 951 | 3,1 |
| 5 | 13506 | 2,8 | 1034 | 3,1 |
Tabelle 2
Intra–Assay–Varianz (n=20)
| Amyloid–beta (1–40) ELISA | Amyloid–beta (1–42) ELISA | |||
| Probe | MW | CV | MW | CV |
| [pg/mL] | [%] | [pg/mL] | [%] | |
| 1 | 2418 | 5,4 | 193 | 4,5 |
| 2 | 3830 | 6,3 | 476 | 7,6 |
| 3 | 19407 | 4,1 | 661 | 6,9 |
| 4 | 13164 | 5,8 | 728 | 4,7 |
| 5 | 9405 | 2,7 | 873 | 7,4 |
Tabelle 3
Inter–Lot– und –Benutzer–Varianz (n=10, 3 Lots, 3–4 Benutzer)
Ein Methodenvergleich mit einem anderen kommerziell verfügbarem Amyloid–beta (1–40)ELISA zeigt eine hervorragende Korrelation mit R2=0.944
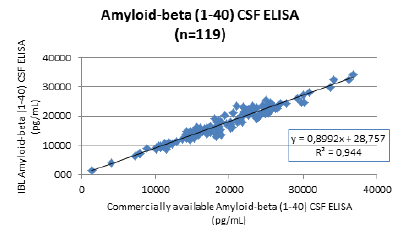 Grafik 1:
Grafik 1:
Methodenvergleich für die Bestimmung von Amyloid–beta (1–40) in 119 nativen Liquorproben
Ein Methodenvergleich mit einem anderen kommerziell verfügbarem Amyloid–beta (1–42) ELISA zeigt eine hervorragende Korrelation mit R2 =0.9492
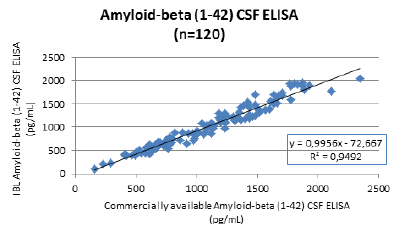 Grafik 2:
Grafik 2:
Methodenvergleich für die Bestimmung von Amyloid–beta (1–42) in 120 nativen Liquorproben
Um die beiden Assays klinischen zu validieren wurde eine externe Studie an der "Klinik und Poliklinik für Psychiatrie und Psychotherapie, Klinikum rechts der Isar der Technischen Universität München, München, Germany" mit insgesamt 83 klinisch gesicherten Proben durchgeführt. Das Ratio aus den Werten beider Assays zeigt hohe klinische Sensitivität und Spezifität
Amyloid–beta (1–42) ⁄ Amyloid–beta (1–40)–Ratio ist der einzelnen Amyloid–beta (1–42) Bestimmung überlegen
| Ratio: Amyloid–beta (1–42) ⁄ Amyloid–beta (1–40) | |||
| AD | Kontrolle | ||
| Diagnose | AD | 39 | 1 |
| Kontrolle | 4 | 39 | |
Ähnliche Ergebnisse wurden am Universitätsklinikum Erlangen erzielt. Diese werden demnächst separat publiziert.
Weltweit wurde die Zahl der Demenzkranken im Jahr 2010 auf 36 Millionen geschätzt. Angenommen, es bleibt beim Mangel an effektiven Präventions- und Heilungsmöglichkeiten, wird alle 20 Jahre eine Verdoppelung der Zahl an Demenzerkrankungen erwartet. Die Alzheimer-Erkrankung ist dabei mit rund 60-70% die häufigste Ursache einer Demenz. Prävalenz und Inzidenz steigen mit zunehmendem Alter. So liegt die Prävalenz bei knapp über 1% bei den 65-69-Jährigen und bei über 30% bei Personen, die 90 Jahre und älter sind.
Der Krankheitsverlauf einer Alzheimer-Erkrankung wird durch 3 Stadien charakterisiert, wie sie durch Arbeitsgruppen des US National Institutes of Aging definiert wurden, das präklinische Stadium, das MCI-Stadium („mild cognitive impairment“, milde kognitive Beeinträchtigung) und das Demenz-Stadium. Schon im präklinischen Stadium kommt es zur Amyloidose. Erste kognitive Defizite werden im MCI-Stadium evident, während in der finalen Demenz der Patient nicht mehr in der Lage ist, zu arbeiten bzw. Alltagstätigkeiten zu verrichten.
Die Konzentration von Amyloid-beta (1-42) im Liquor wird daher als sehr hilfreicher Biomarker in der Diagnose der Alzheimer-Erkrankung angesehen (in Kombination mit anderen Biomarkern wie Tau und Phospho-Tau). Darüber hinaus wurde das Ratio von Amyloid-beta (1-42) zu Amyloid-beta (1-40) in mehreren unabhängigen Studien als überlegener diagnostischer Marker im Vergleich zum Amyloid-beta (1-42) allein für die Alzheimer-Erkrankung gezeigt (Literatur-Referenzen verfügbar).
Für konkrete Daten konsultieren Sie bitte die Arbeitsanweisung in der Download Box oben auf der rechten Seite.
Zu unserem umfassenden Angebot an Immunassays gehören eine Reihe spezialisierter diagnostischer Immunassays für die Endokrinologie, Immunologie und zur Untersuchung von Autoimmunkrankheiten, sowie zur Diagnose von zahlreichen Infektionskrankheiten. Wir sind Pioniere und Marktführer in der Speicheldiagnostik, und bieten seit über 40 Jahren ein breites Portfolio an Lumineszenz- und ELISA-basierten Tests.
Als Experten im Bereich Laborautomation unterstützen wir unsere Kunden mit Protokollen für offene ELISA-Plattformen wie dem Freedom EVOlyzer oder dem Thunderbolt®.
Sämtliche Produkte sind nur für den Verkauf an Laborpersonal verfügbar und möglicherweise nicht in allen Ländern erhältlich. Bitte lesen und befolgen Sie immer die Arbeitsanleitung. Kontaktieren Sie uns gerne für weitere Informationen.
Design und Herstellung aller unserer Assays erfüllen die höchsten Anforderungen globaler Richtlinien und Qualitätsstandards. Tecan ist unter ISO 9001:2015, ISO 13485:2016 zertifiziert und gemäß Medical Device Single Audit Program (MDSAP) von einer Benannten Stelle auditiert.

Als Teil der Tecan-Gruppe haben wir eine führende Marktposition in Diagnostik und Forschung. Wir verfügen über 40 Jahre Erfahrung in der Entwicklung, Herstellung und Bereitstellung von Immunassays auf Basis von Enzymreaktionen, Radiomarkierungen und Lumineszenz.
Unsere Bandbreite hochqualitativer Immunassays wird durch ein vielfältiges Portfolio automatisierter Lösungen ergänzt. So sind wir der perfekte Partner für Sie und Ihre Kunden.
At Tecan, we are driven to improve people’s lives and health.