IGFBP-3 ELISA
- Regulatorischer Status
- EU: CE
- Kit Größe
- 12 x 8
- Methode
- ELISA
- Inkubationszeit
- 2 x 1 hr,1 x 30 min
- Standardbereich
- 0.4 - 15150 µg/L
- Probe / Vorbehandlung
- 10 µl Serum, Plasma
- Substrat / Isotop
- TMB, 450 nm
Quantitative Messung von humanem insulinähnlichem Wachstumsfaktor 3 (IGFBP-3) in menschlichem Serum oder EDTA- und Heparin-Plasma für diagnostische und wissenschaftliche Zwecke.
Insulin-like growth factors (IGF)-I und -II sind im Blutkreislauf an spezielle Bindungsproteine (IGFBPs) gebunden. Bisher wurden sechs verschiedene Bindungsproteine anhand ihrer Aminosäuresequenz identifiziert und als IGFBP-1, IGFBP-2, ..., IGFBP-6 klassifiziert (1). Im Blut überwiegt IGFBP-3, das hauptsächlich zur Regulierung der IGF-I und -II Konzentrationen dient. Im Gegensatz zu den anderen Bindungsproteinen hat IGFBP-3 die Eigenschaft, neben IGF-I bzw. -II noch eine säurelabile Untereinheit (acid-labile subunit, ALS) zu binden (3-5). IGFBP-3 liegt fast vollständig in Form dieses hochmolekularen ternären Komplexes vor, es finden sich aber auch geringe Mengen freies IGFBP-3 im Blut (6,7).
Die Entwicklung spezifischer Immunoassays, die IGFBP-3 auch im ternären Komplex erkennen, ermöglichte neue Einsichten in die Regulation dieses Proteins (6-9). Demnach erwies sich IGFBP-3 als nützlicher Parameter bei der Diagnose von Wachstumsstörungen (7,8).
Jedoch wird die IGFBP-3 Konzentration nicht nur vom Wachstumshormon sondern auch von weiteren Faktoren beeinflusst: Alter und sexuelles Entwicklungsstadium, Ernährung, Hypothyreose, Diabetes mellitus, Leber- und Nierenfunktion. IGFBP-3 Werte sind erniedrigt bei Unterernährung, bei Hypothyreose, Diabetes mellitus und Lebererkrankungen (6-8). Bei Vorliegen einer chronischen Niereninsuffizienz liegen jedoch erhöhte Konzentrationen vor (6,10,11). 24-Stunden-Messungen zeigen keine zirkadianen Schwankungen (12,13). Für klinische Belange ist der wichtigste regulierende Faktor das Wachstumshormon. IGFBP-3- Einzelmessungen korrelieren positiv mit dem Logarithmus der spontanen Gesamt-WH- Sekretion (8,14). Bei Patienten mit WH-Mangel sind auch die IGFBP-3 Werte erniedrigt. Mehrere Tage nach Beginn einer WH Therapie steigt die IGFBP-3 Konzentration langsam bis in den normalen Bereich an (7,8).
Die langsame Reaktion auf WH- Konzentrationsänderungen und konstante zirkadiane Werte während täglicher WH-Gabe (13) lassen die Vermutung zu, dass IGFBP-3 den WH-Sekretionsstatus über mehrere Tage widerspiegelt.
Die großen Vorteile der IGFBP-3 Messung verglichen mit der IGF-I Messung sind:
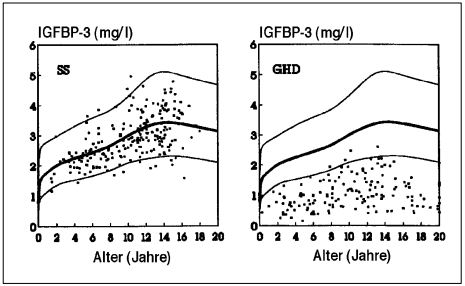
Abb. 1: IGFBP-3 Serumwerte bei kleinwüchsigen Patienten ohne WH-Mangel: angeborene Wachstumsund Entwicklungsverzögerung, vererbte Kleinwüchsigkeit, intra-uterine Wachstumsverzögerung (SS: short stature) sowie bei idiopathischem oder organischem WH-Mangel (GHD: growth hormone deficiency). Der Normalbereich ist durch die 5. und 95. Perzentile definiert.
Abb. 2: IGFBP-3 Serumwerte bei Kindern mit WH-Mangel vor und während der Behandlung mit WH.

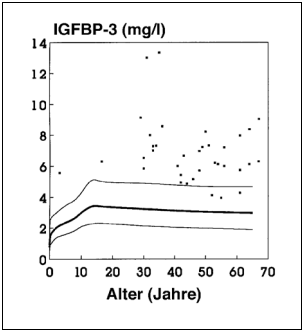
Bei normalwüchsigen Kindern und Jugendlichen oder bei Patienten mit Sotos-Syndrom sind die IGFBP-3 Werte normal oder leicht erhöht. Im Gegensatz dazu sind die Werte bei Kindern mit Gigantismus oder Erwachsenen mit Akromegalie stark erhöht (Abbildung 3) (6,15) und normalisieren sich nach erfolgreicher Behandlung. Daher ist die IGFBP-3- Messung auch hier ein nützlicher Parameter zur Diagnose von WHÜberschuss und Überwachung des Behandlungserfolgs. Bei frühreifen Kindern sind die IGFBP-3-Werte deutlich erhöht, während sie sich bei Patientinnen mit verfrühter Thelarche im oberen Normalbereich bewegen (15).
Abb. 3: IGFBP-3 Serumwerte bei Akromegalie. Der Normalbereich ist durch die 5., 50. und 95. Perzentile definiert.
Für konkrete Daten konsultieren Sie bitte die Arbeitsanweisung in der Download Box oben auf der rechten Seite.
Zu unserem umfassenden Angebot an Immunassays gehören eine Reihe spezialisierter diagnostischer Immunassays für die Endokrinologie, Immunologie und zur Untersuchung von Autoimmunkrankheiten, sowie zur Diagnose von zahlreichen Infektionskrankheiten. Wir sind Pioniere und Marktführer in der Speicheldiagnostik, und bieten seit über 40 Jahren ein breites Portfolio an Lumineszenz- und ELISA-basierten Tests.
Als Experten im Bereich Laborautomation unterstützen wir unsere Kunden mit Protokollen für offene ELISA-Plattformen wie dem Freedom EVOlyzer oder dem Thunderbolt®.
Sämtliche Produkte sind nur für den Verkauf an Laborpersonal verfügbar und möglicherweise nicht in allen Ländern erhältlich. Bitte lesen und befolgen Sie immer die Arbeitsanleitung. Kontaktieren Sie uns gerne für weitere Informationen.
Design und Herstellung aller unserer Assays erfüllen die höchsten Anforderungen globaler Richtlinien und Qualitätsstandards. Tecan ist unter ISO 9001:2015, ISO 13485:2016 zertifiziert und gemäß Medical Device Single Audit Program (MDSAP) von einer Benannten Stelle auditiert.

Als Teil der Tecan-Gruppe haben wir eine führende Marktposition in Diagnostik und Forschung. Wir verfügen über 40 Jahre Erfahrung in der Entwicklung, Herstellung und Bereitstellung von Immunassays auf Basis von Enzymreaktionen, Radiomarkierungen und Lumineszenz.
Unsere Bandbreite hochqualitativer Immunassays wird durch ein vielfältiges Portfolio automatisierter Lösungen ergänzt. So sind wir der perfekte Partner für Sie und Ihre Kunden.
At Tecan, we are driven to improve people’s lives and health.