IBL International bietet im Produktbereich für Tropenkrankheiten jetzt einen neuen ELISA für den Nachweis einer Zikavirus Infektion an, eine sich gegenwärtig dramatisch ausbreitende Infektion in Latein Amerika und der Pacific Region.
Das Zikavirus, ein RNA virus aus der Familie der Flaviviridae, wird meist von Mücken der Gattung Aedes übertragen. Seit Mai 2015 gibt es einen massenhaften Ausbruch, der in Brasilien seinen Anfang nahm. Seit Oktober 2015 breitet sich das Virus auf weitere Länder und Gebiete insbesondere in Latein Amerika aus. Millionen von Menschen haben sich nach jetzigen Schätzungen angesteckt. Die Weltgesundheitsorganisation WHO hat das Zikavirus als eine internationale Gesundheitsbedrohung eingestuft, insbesondere durch das Risiko von Fehlbildungen bei Kindern infizierter Frauen. Mehr als 4 Millionen Menschen könnten sich bis Ende 2016 mit dem Virus infiziert haben.
Die Symptome ähneln denen anderer mückenübertragender Infektionen (z.B. Denguefieber oder Chikungunyafieber). Am häufigsten sind Hautausschlag, Kopf-, Gelenk- und Muskelschmerzen, Bindehautentzündung und Fieber. Schwangere bilden eine besondere Risikogruppe, da ein kausaler Zusammenhang zwischen einer Zikavirus-Infektion in der Schwangerschaft und Hirnfehlbildungen beim ungeborenen Kind besteht.
Durch dieses Gefährdungspotenzial kommt der Diagnostik eine besondere Bedeutung zu. Abgesehen von einer symptomatischen Diagnose basierend auf dem Aufenthalt in Ausbruchsgebieten, lässt sich eine Zikavirus-Infektion im Blut und im Urin entweder direkt nachweisen (PCR) oder etwas später über eine Antikörper-Diagnostik.
IBL International bietet zu diesem Zweck jetzt einen ELISA für die Bestimmung von IgM Antikörpern basierend auf der sehr sensitiven und spezifischen µ-capture Technologie an.
Der ELISA bietet Ihnen folgende Besonderheiten:
- Diagnose einer Zikavirus Infektion
- µ-capture Technologie
- Sehr geringe Kreuzreaktivität zu anderen Flaviviridae
- Qualitative Auswertung
- Sensitivität > 99%, Spezifität 98.5%
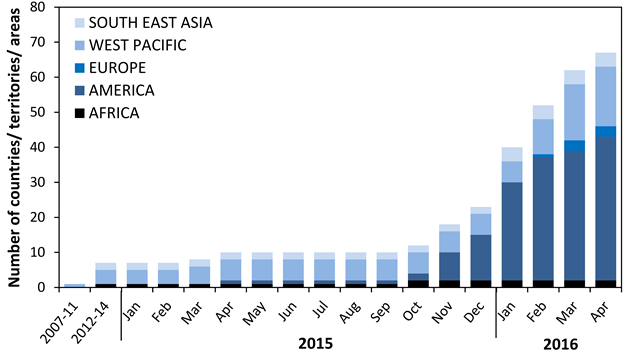
Anzahl der Länder und Gebiete mit Zikavirus Infektionen, Jahre 2007-2016
Bestimmung der diagnostischen Leistungsfähigkeit des Tests
Messung von 140 Proben:
9 positive Zika virus Proben (BNI Hamburg, Germany)
47 negative Proben (Blutbank Frankfurt, Germany)
84 Proben zur Überprüfung der Kreuzreaktivität (United States, Uganda, Guadeloupe, New Caledonia)
| Definierter Probenstatus |
| positiv | negativ | ∑ |
| IBL Zika virus IGM µ-capture ELISA | positiv | 9 | 0 | 9 |
| negativ | 0 | 129 | 129 |
| ∑ | 9 | 129 | 138 |
The IBL Zika virus IgM µ-capture ELISA zeigt eine 98.6%ige (138/140) Übereinstimmung des Messergebnisses mit dem vordefinierten Probenstatus..
Auszug aus der Arbeitsanleitung
Testprinzip
Die qualitative immunenzymatische Bestimmung von spezifischen IgM-Antikörpern beruht auf der ELISA (Enzyme-linked Immunosorbent Assay) μ-capture Technik. Die Mikrotiterplatten sind mit anti-human IgM-Antikörpern beschichtet, an welche die korrespondierenden Antikörper aus der Probe binden. Ungebundenes Probenmaterial wird durch Waschen entfernt. Anschließend erfolgt die Zugabe eines Meerettich-Peroxidase (HRP) konjugierten Zikavirus Antigens. Dieses Antigen-Konjugat bindet an die an der Mikrotiterplatte gebundenen spezifischen IgM-Antikörper. In einem zweiten Waschschritt wird ungebundenes Konjugat entfernt. Die Immunkomplexe, die durch die Bindung des Konjugates entstanden sind, werden durch die Zugabe von Tetramethylbenzidin (TMB)-Substratlösung und eine resultierende Blaufärbung nachgewiesen. Die Intensität des Reaktionsproduktes ist proportional zur Menge der spezifischen IgM-Antikörper in der Probe. Die Reaktion wird mit Schwefelsäure gestoppt, wodurch ein Farbumschlag von blau nach gelb erfolgt. Die Absorption wird bei 450/620 nm mit einem Mikrotiterplatten-Photometer gemessen.
Vertrieben durch Tecan, IBL International GmbH.
Für konkrete Daten konsultieren Sie bitte die Arbeitsanweisung in der Download Box oben auf der rechten Seite.