17-OH-Progesteron ELISA
- Regulatorischer Status
- EU: CE IVDR
- Kit Größe
- 12 x 8
- Methode
- ELISA
- Inkubationszeit
- 1 x 60 min, 1 x 30 min
- Standardbereich
- 0.15 - 20 ng/mL
- Probe / Vorbehandlung
- 25 µL serum, plasma
- Substrat / Isotop
- TMB 450 nm
Verwendungszweck
Enzymimmunoassay zur quantitativen in-vitro-Diagnostik von 17-OH-Progesteron in Humanserum und EDTA-Plasma von Frauen, Männern und Kindern. Dieser Test dient als Hilfsmittel zur Diagnose und Überwachung der kongenitalen adrenalen Hyperplasie, bei der aufgrund eines genetischen 21-Hydroxylase-Mangels erhöhte 17-OH-Progesteron-Spiegel im Vergleich zu einer entsprechenden Population scheinbar gesunder Personen festgestellt werden. Zusätzlich werden andere klinische Steroidhormone (Androstendion und Cortisol) und genetische Tests eingesetzt, um den Status der kongenitalen adrenalen Hyperplasie zu beurteilen. Dieser Test ist als Hilfsmittel für die Diagnose und Überwachung der späten kongenitalen adrenalen Hyperplasie gedacht, bei der die 17-OH-Progesteron-Spiegel im Vergleich zu einer entsprechenden Population scheinbar gesunder Individuen aufgrund von Störungen (21-Hydroxylase-Mangel oder Androgen-"Hintertür"-Weg) im Metabolismus von 17-OH-Progesteron, die zur Akkumulation dieses Steroids führen, erhöht sind. Zusätzlich werden andere klinische Beobachtungen wie körperliche Untersuchungen, die Quantifizierung anderer Steroidhormone (Androstendion, Cortisol und Dihydrotestosteron) und genetische Tests eingesetzt, um den Status der spät einsetzenden kongenitalen Nebennierenhyperplasie zu beurteilen. In bestimmten Fällen einer kongenitalen Nebennierenhyperplasie werden die 17-OH-Progesteron-Spiegel vor und nach der Stimulation mit ACTH quantifiziert. Der 17-OH-Progesteron-ELISA ist NICHT zur Verwendung im Neugeborenen- Screening und zur Überwachung von Patienten mit hypogonadotropem Hypogonadismus geeignet.
Der 17-OH-Progesteron-ELISA ist ein Festphasen-Enzymimmunoassay (ELISA), der auf dem Prinzip der kompetitiven Bindung basiert und mit einem Absorptionslesegerät gemessen wird. Der Assay kann vom Laborpersonal auf offenen ELISA-basierten Liquid-Handler-Plattformen automatisiert werden; die Programmierung der Schritte und das Timing, die in den Testanweisungen des manuellen Kits vorgeschrieben sind, müssen jedoch streng eingehalten und vom Labor überprüft werden. Die Testergebnisse können manuell anhand einer Standardkurve berechnet und mit im Labor festgelegten Referenzbereichen von gesunden Erwachsenen (d. h. Normalbereichen) verglichen werden. Das Testkit ist für den professionellen Laborgebrauch durch geschultes Personal vorgesehen. Das Testkit ist nicht für den Hausgebrauch oder den Gebrauch durch Laien bestimmt.
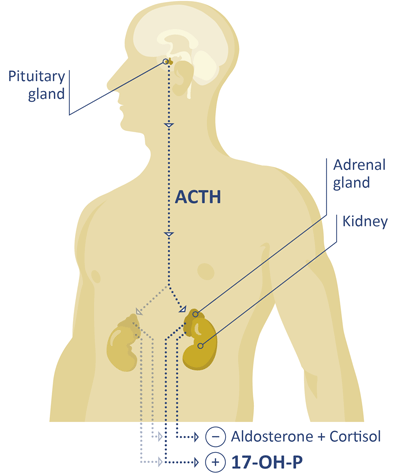
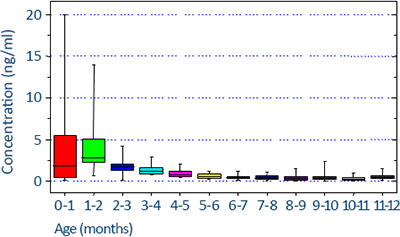
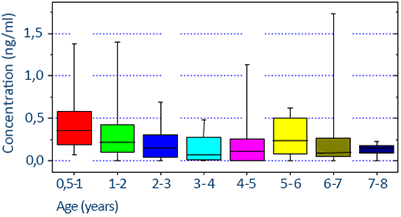
Klinische Bedeutung
17-Hydroxyprogesteron (17-OHP) ist ein Steroidhormon, das im menschlichen Körper im Kreislauf zu finden ist. Die Rolle von 17-OHP als Zwischenprodukt in der Biosynthese von Cortisol ist in der wissenschaftlichen Literatur gut belegt.[2] Die Quantifizierung von 17-OHP aus Serum oder Plasma kann als Hilfsmittel bei der Diagnose oder Überwachung der kongenitalen Nebennierenhyperplasie (CAH) und der nicht-klassischen kongenitalen Nebennierenhyperplasie (NCCAH) verwendet werden. Diese Erkrankungen sind mit Defiziten in der Aktivität der 21-Hydroxylase verbunden. Dieses Enzym metabolisiert 17-OHP auf dem Weg zu Cortisol. Die Identifizierung von 17-OHP als Biomarker für CAH und NCCAH ist konsistent mit der Blockade des biochemischen Weges der Cortisol Produktion. In der gestörten Biosynthese ist 17-OHP das letzte Zwischenprodukt vor dem dysfunktionalen Enzym (21-Hydroxylase, P450c21). Ein Konzentrationsanstieg ist die Folge des stetigen Zuflusses durch die Umwandlung von Progesteron und 17-OH-Pregnenolon zu 17-OHP. Gesunde Patienten können identifiziert werden, wenn ihre 17-OHP-Spiegel innerhalb der jeweiligen Referenzbereiche liegen.[1] Die 17-OHP-Spiegel unterliegen Schwankungen. Die Proben sollten bei allen Patienten am frühen Morgen entnommen werden. Eine besondere Anforderung besteht für menstruierende Frauen; ihre Proben sollten in der Follikelphase entnommen werden. 17-OHP-Spiegel, die unter diesen Einschränkungen quantifiziert wurden, gelten als "Baseline"-Spiegel. Patienten, die von CAH oder NCCAH betroffen sind, können mit 17-OHP-Werten oberhalb der jeweiligen Referenzbereiche identifiziert werden. Kliniker sollten hohe 17-OHP-Spiegel, die auf CAH hindeuten können, bestätigen, z. B. mit Hilfe der Gold-Standard-Methode (LC-MS), durch Untersuchung der 17-OHP-Spiegel nach Cosyntropin-Stimulation oder durch genetische Tests. Die Überwachung von Patienten mit CAH ist nicht allein vom 17-OHP-Spiegel abhängig, sondern umfasst auch die Untersuchung anderer Hormone. Ziel der medikamentösen Behandlung ist es, den Überschuss an androgenen Hormonen zu unterdrücken.[4] Daher wird eine regelmäßige Messung der Androgene (Testosteron, Androstendion) empfohlen.[3] Für die Überwachung von NCCAH-Patienten dürfen die bei der Analyse gewonnenen Werte nicht unbedingt in Korrelation zu einem Referenzbereich betrachtet werden, sondern im Hinblick auf die Krankengeschichte des Betroffenen.
Produktverfügbarkeit und regulatorischer Status können außerhalb der EU je nach länderspezifischer Registrierung variieren. CE IVD unter IVDR wird demnächst eingeführt. Wenden Sie sich für weitere Informationen an Ihren Tecan-Partner.
Für konkrete Daten konsultieren Sie bitte die Arbeitsanweisung in der Download Box oben auf der rechten Seite.
Zu unserem umfassenden Angebot an Immunassays gehören eine Reihe spezialisierter diagnostischer Immunassays für die Endokrinologie, Immunologie und zur Untersuchung von Autoimmunkrankheiten, sowie zur Diagnose von zahlreichen Infektionskrankheiten. Wir sind Pioniere und Marktführer in der Speicheldiagnostik, und bieten seit über 40 Jahren ein breites Portfolio an Lumineszenz- und ELISA-basierten Tests.
Als Experten im Bereich Laborautomation unterstützen wir unsere Kunden mit Protokollen für offene ELISA-Plattformen wie dem Freedom EVOlyzer oder dem Thunderbolt®.
Sämtliche Produkte sind nur für den Verkauf an Laborpersonal verfügbar und möglicherweise nicht in allen Ländern erhältlich. Bitte lesen und befolgen Sie immer die Arbeitsanleitung. Kontaktieren Sie uns gerne für weitere Informationen.
Design und Herstellung aller unserer Assays erfüllen die höchsten Anforderungen globaler Richtlinien und Qualitätsstandards. Tecan ist unter ISO 9001:2015, ISO 13485:2016 zertifiziert und gemäß Medical Device Single Audit Program (MDSAP) von einer Benannten Stelle auditiert.

Als Teil der Tecan-Gruppe haben wir eine führende Marktposition in Diagnostik und Forschung. Wir verfügen über 40 Jahre Erfahrung in der Entwicklung, Herstellung und Bereitstellung von Immunassays auf Basis von Enzymreaktionen, Radiomarkierungen und Lumineszenz.
Unsere Bandbreite hochqualitativer Immunassays wird durch ein vielfältiges Portfolio automatisierter Lösungen ergänzt. So sind wir der perfekte Partner für Sie und Ihre Kunden.
At Tecan, we are driven to improve people’s lives and health.